梓梦-美国药典USP788 与中国药典0903(2025年版)不溶性微粒检测对比分析--共同点

一、核心定位与整体框架
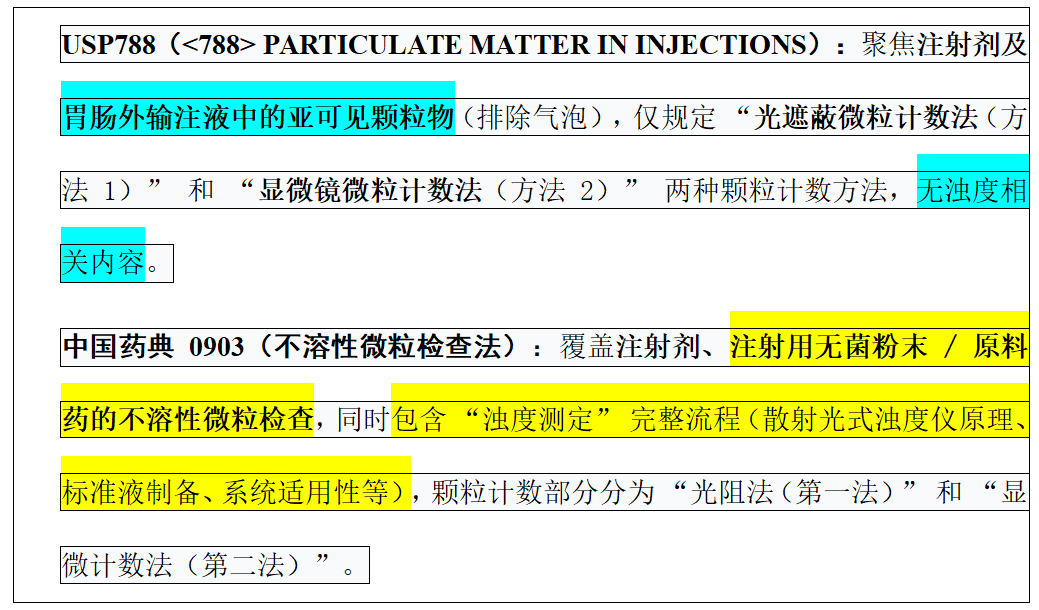
二、共同点
1. 检查目的与检测对象一致


2. 核心检测方法类型与原理相似
两者均采用 “光阻 / 光遮蔽类方法" 和 “显微镜计数类方法" 作为颗粒计数的核心技术,原理高度一致:

3. 样品处理与操作共性

4. 环境与器具质量控制一致
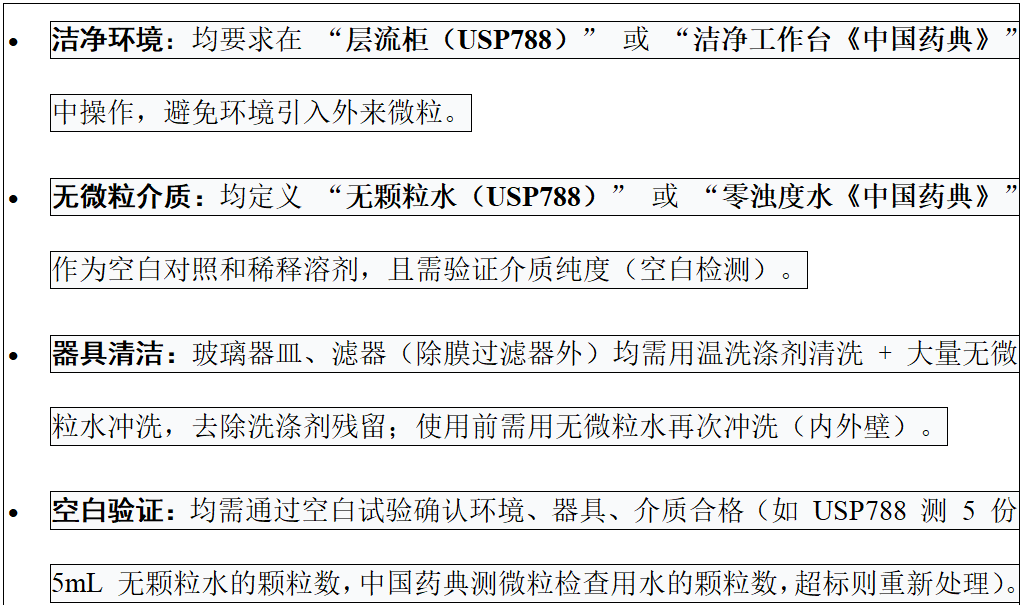
5. 结果判定逻辑与限度数值一致
两者均按 “标示装量是否≥100mL" 分档设定颗粒限度,且同类型方法的限度数值相同:
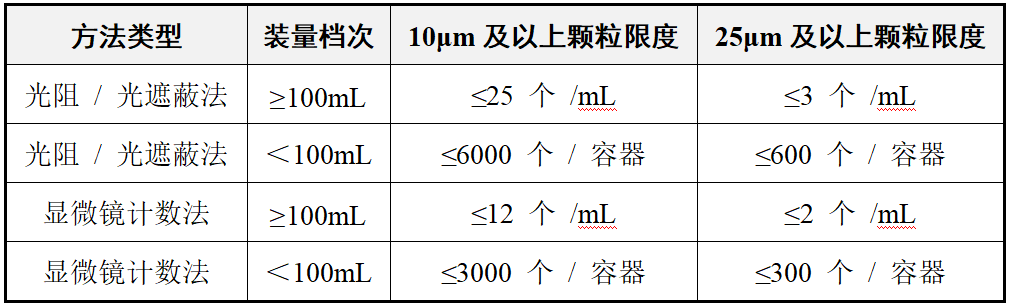
方法互补性:均规定 “光阻 / 光遮蔽法结果超标时,需用显微镜计数法复核,并以显微镜法结果作为最终判定依据"。
6. 抽样与统计要求一致
均强调 “统计学合理的取样计划":样品数量需足够支撑可靠评估(如大容量注射剂或≥25mL 小容量注射剂,可根据取样计划测试少于 10 个单位),且单批检测结果不可直接外推至未测试单位。
简言之,两者在 “颗粒计数" 的核心技术和质量控制逻辑上高度统一,但中国药典通过细化仪器校准规范、完善特殊样品处理流程、建立浊度测定体系等方式,进一步提升了方法的严谨性与适用性,为药品颗粒污染控制提供了更具操作性的技术指导。